
CNEWS匯流新聞網記者謝東明、李盛雯/台北報導
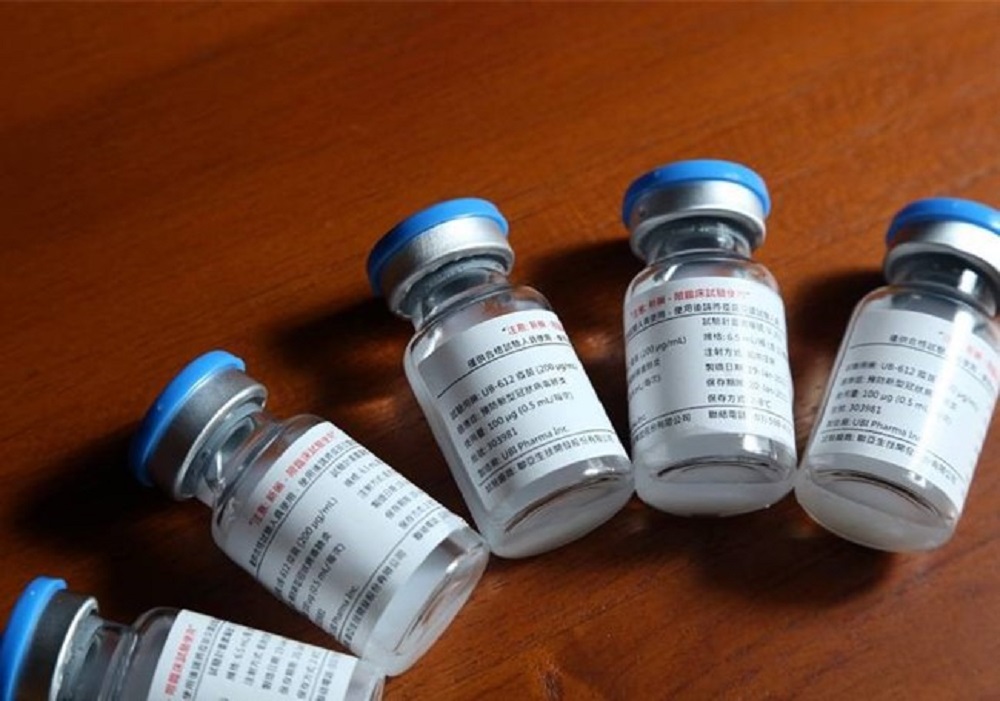
聯亞生技宣布,董事長王長怡帶領團隊一手催生的UB-612新冠疫苗,在接受流行病預防創新聯盟執行美國FDA核准之多國多中心臨床三期試驗,今年9月底完成收案,並於12月2日發佈攸關藥物能否批准上市的「樞紐試驗」(pivotal studies),以不劣性的試驗達成各項指標,進入新藥研發過程中的最後一哩路。
聯亞生技表示,預計在 2023 年上半年向英國藥品和醫療產品監管署和澳洲治療產品管理局提交有條件/臨時批准營銷申請許可,並可望列入世界衛生組織(WHO)的緊急使用清單(EUL)。
聯亞生技指出,此三期臨床試驗,旨在UB-612以異源混打追加劑 (heterologous booster)之形式,比較當今已通過WHO核准市售流通最廣用的三類疫苗(全球已達35億人口接種)的同源追加劑(homologous booster),以主要和關鍵的次要免疫原性終點(immunogenicity endpoints)評比,成功達標:UB-612與mRNA(輝瑞-BioNTech 的 BNT162b2)、腺病毒載體(阿斯利康 AZ的 ChAdOx1- S)、滅活病毒(國藥BIBP)疫苗相比,針對Wuhan(原始武漢株)和Omicron BA.5變體病毒,產生更優異的中和抗體滴度和血清轉化率。
而且UB-612仍然呈現相當好的安全及耐受性,總試驗將於2023年下半年結束,並提供有關T細胞免疫力和免疫反應持久性等更多長期數據。結論顯示,UB-612將是在新冠疫情流感化後,為廣大已接種各類疫苗的人口,提供絕佳的疫苗選擇。
在台灣由聯亞生技執行的3875人擴大臨床二期試驗及1378人追加劑延伸試驗,已證明UB-612疫苗具備良好的免疫原性及安全性,且具備獨特的T細胞免疫效能、中和抗體持續性長久、具強烈免疫記憶性、可對抗各種新冠變異病毒之廣效特性。此次臨床三期試驗,更證明UB-612追加劑可快速加強產生對抗原始病毒與Omicron等變異株的高效價抗體,將可提高對抗新冠病毒變異株之混打接種策略之彈性。
聯亞生技指出,至今全球新冠疫苗施打率第一劑基礎針達64.7%、第二劑基礎針達58.2%、追加劑(第三劑)達21.7%。但低收入國家僅14.8% 的人接受過一劑疫苗,施打率遠不及全球平均。加上新冠病毒快速變異與肆虐,目前其他類型疫苗恐因抗體效價半衰期短,需持續施打以造成免疫疲乏而失效。
在各國紛紛開啟國門之際,希望UB-612能用以防範未來不斷變異病毒,導致疫情失控的隱憂,並可透過具高度T細胞免疫性的UB-612降低長新冠後遺症。期望透過創新B + T全方位免疫反應的UB-612疫苗協防全球抗疫。
照片來源:翻攝聯亞生技官網、聯亞生技提供
更多匯流新聞網報導:
946噸醜蔬果和肉品不浪費 新北105惜食點造福逾137萬人次
【文章轉載請註明出處】
延伸閱讀
【CNEWS】揭柯文哲「3件事」不夠決斷!林濁水曝做到「這點」綠死無退路
- 2025-01-20
- 林 佑威
【CNEWS】就業安定基金遭濫用?洪申翰「這樣說」林淑芬變臉「又要吐了」批獨厚綠能
- 2024-12-05
- 林 佑威
海關扣留包裹 8旬老翁險遭詐百萬元
- 2024-04-16
- 謝 東明
