匯流新聞網記者陳鈞凱/台北報導
賣到各大醫療院所的生理食鹽水注射液出包!食藥署今(31)日發布最新產品回收訊息,接獲永豐化學工業股份有限公司通報,旗下生產的「”永豐”生理食鹽水注射液」100mL軟袋裝,安定性試驗的pH值測定結果未能符合規格,共有35批號產品得回收。
出問題的「”永豐”生理食鹽水注射液」問題批號,包括:107D03E、107D04E、107D05E、107D06E、107D07E、107D08E、107D09E、107D10E、107D11E、107D12E、107D13E、107D14E、107D15E、107D16E、107D17E、107D18E、107D19E、107D20E、107D21E、107D22E、107D23E、107D24E、107D25E、107D26E、107D27E、107D28E、107D29E、107D30E、107D31E、107D32E、107D33E、107D34E、107D35E、107D36E、107D37E(100mL軟袋裝效期內全批號)。
食藥署品質監督管理組組長遲蘭慧表示,這些100mL軟袋裝的生理食鹽水屬於注射劑型,多銷向各大醫療院所,做為注射液或用來調配藥品之用,廠商是在針對部分批號產品進行第11個月安定性試驗時,發現pH值測定結果未能符合規格的4.5到7範圍內,數值低於4.5偏酸,因此廠商通報主動回收。
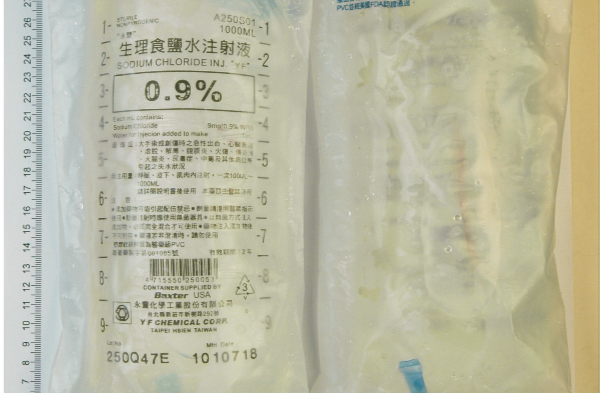
「”永豐”生理食鹽水注射液」主成分為SODIUM CHLORIDE。根據食藥署核准適應症為:大手術或創傷時之急性出血、心臟衰弱、虛脫、解毒、腹膜炎、炎傷、傳染病、大腸炎、尿毒症、中毒及其他病症所引起之失水狀況。
遲蘭慧強調,目前已要求廠商得在5月19日前全面回收,問題批號的總數量還待查,且有部分尚未出廠;食藥署同時要求廠商得繳交調查報告,查明原因,食藥署亦會展開不定期抽查,確保相關藥品品質無虞。
照片來源:食藥署提供
更多匯流新聞網報導:
首曝光!國人接種AZ疫苗兩大症狀最多 7.8%第一天不適到無法工作
美國返台7旬翁「在台活動已2個半月」 出境前一刻才被發現確診
【文章轉載請註明出處】
延伸閱讀
廣告膨風新北開鍘逾7000萬元 違規產品以食品占大宗
- 2025-03-11
- 謝 東明
藥品開封乾燥劑該留還是丟?藥師揭正確保存關鍵
- 2025-02-07
- 李 映萱
合歡山雪季 新城警籲上山前請落實相關賞雪措施
- 2024-12-26
- 謝 東明
