匯流新聞網記者陳鈞凱/台北報導
繼嬰幼兒莫德納疫苗7月21日在國內開打之後,食藥署今(1)日宣布專案核准Pfizer-BioNTech幼兒疫苗可以用於6個月至4歲幼兒接種以預防COVID-19;用法用量為施打3劑,前2劑施打間隔至少21天,第2劑後間隔至少8周再施打第3劑。
食藥署是在7月29日召開專家會議,討論是否同意核准Pfizer-BioNTech疫苗適用於6個月至4歲兒童的主動免疫接種以預防COVID-19,最後准了。
食藥署表示,經審查Pfizer-BioNTech疫苗在6個月至4歲兒童所進行的一項第一、二、三期臨床試驗結果,試驗結果顯示6個月至4歲兒童試驗組所誘發的中和抗體免疫原性結果,不劣於青少年及成人試驗組的免疫原性結果;安全性方面,與其他年齡組別相比,沒有新增的安全性疑慮。
食藥署說,經整體評估其有效性及安全性,考量國內緊急公共衛生需求,與會專家建議專案核准Pfizer-BioNTech幼兒疫苗適用於6個月至4歲兒童的基礎接種,用法用量為施打3劑,每劑0.2毫升(含3微克的mRNA),前2劑施打間隔至少21天,第2劑後間隔至少8周再施打第3劑。
食藥署表示,在臨床試驗中,6個月至未滿2歲兒童接種任一劑疫苗最常見的不良反應包括躁動、食慾下降、注射部位壓痛、注射部位發紅、發燒和注射部位腫脹等,而2至4歲兒童最常見的不良反應包括注射部位疼痛、疲勞、注射部位發紅、發燒和頭痛等,臨床試驗中沒有發現有心肌炎、心包膜炎或死亡案例。未來食藥署將持續監控國內外接種COVID-19疫苗的安全警訊,分析評估疫苗不良事件通報資料,執行安全監視機制,保障民眾接種疫苗之安全。
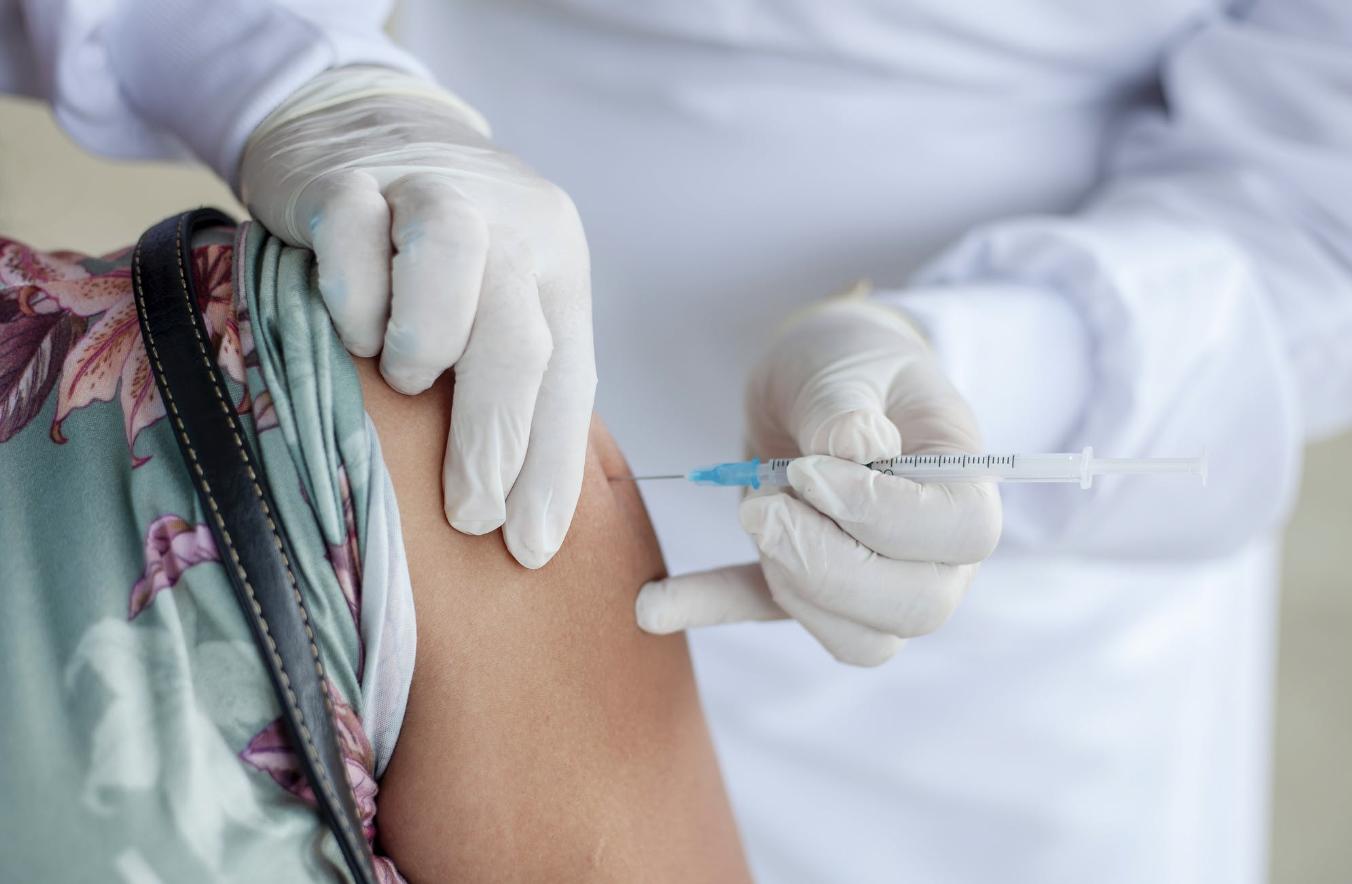
照片來源:示意照/翻攝自Pexels
更多匯流新聞網報導:
【文章轉載請註明出處】
延伸閱讀
罐裝可樂出包「恐致腎衰竭」香港、英國都召回! 食藥署:台灣沒進口
- 2025-03-27
- 陳 鈞凱
食不安!北海道進口「烏賊」重金屬鎘超標 泰國2款果乾漂白劑違規
- 2025-03-25
- 陳 鈞凱
非法假牙恐致癌、慢性中毒 林月琴譴責食藥署自廢武功
- 2025-03-14
- 邱 璽臣
